Von Myosin-Motoren und Nukleator-Proteinen
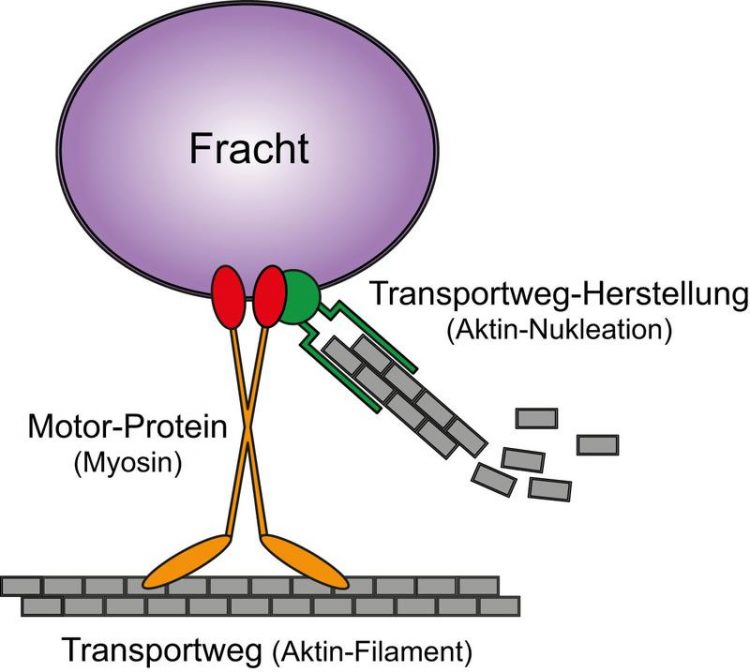
Modell der Aktin/Myosin-Funktion im Transport. Tobias Welz (Universität Regensburg) - Zur ausschließlichen Verwendung im Rahmen der Berichterstattung zu dieser Pressemitteilung!
Die Zellen des menschlichen Körpers unterscheiden sich in Gestalt und Aufgabe. So sind die weißen Blutkörperchen des Immunsystems eher rund und die Neurone des Gehirns haben eine weitverzweigte, baumartige Struktur.
Zellen bekommen ihre spezifische Form durch den Transport von Proteinen an die Zelloberfläche. Dadurch können sich unterschiedliche Oberflächen und Zellstrukturen aufbauen.
Ein schönes Beispiel ist das Darm-Epithel, eine ebene Zellschicht, in der alle Zellen an den Seiten durch Proteine miteinander verbunden sind. Um Proteine innerhalb der Zelle zu transportieren und genau an den Ort zu bringen, an dem sie benötigt werden, bedienen sich die Zellen sogenannter Motor-Proteine, die mit ihrer Fracht entlang von Filamenten des zellulären Zytoskeletts gleiten.
Neben den größeren Mikrotubuli findet der Transport in Zellen an den dünneren und sehr flexiblen Aktin-Filamenten statt. Motor-Proteine der Myosin-Proteinfamilie transportieren dabei ihre Fracht entlang der Aktin-Filamente.
Ein internationales Team um Prof. Dr. Eugen Kerkhoff, Professur für Genomik und Zellstruktur an der Universität Regensburg, und seinen Assistenten, den Neurowissenschaftler Tobias Welz, hat jetzt einen neuen Proteinkomplex entdeckt, der eine Kopplung von Aktin-Filament Bildung und Motor-Protein Aktivierung aufzeigt.
Sogenannte Aktin-Nukleator Proteine, die die Herstellung der Aktin-Filamente katalysieren, bilden dabei einen Proteinkomplex mit den Myosin-Motoren. Die direkte Interaktion der Nukleator- und Motor-Proteine steuert die Anwesenheit des Proteinkomplexes an Transportbehältern. Dies ermöglicht einen Aktin/Myosin-abhängigen Transport im Inneren der Zellen, abseits des zellstabilisierenden Aktin-Filament-Netzwerks unterhalb der Zellmembran.
Obwohl man die Bandbreite der Funktionen des neuen Proteinkomplexes bisher nur ahnen kann, steht bereits jetzt fest, dass er eine essentielle Rolle in der weiblichen Eizellreifung hat und mit großer Wahrscheinlichkeit auch von grundlegender Bedeutung für Lernprozesse unseres Gehirns ist.
Aus klinischer Sicht ist besonders interessant, dass sich auch Viren und Bakterien dieser Transportmechanismen bedienen, um sich in ihren Wirtszellen zu vermehren. Der Proteinkomplex stellt damit ein mögliches Ziel für neue anti-virale und anti-bakterielle Therapien dar.
Die Ergebnisse wurden in der Zeitschrift „eLife“ veröffentlicht unter:https://elifesciences.org/content/5/e17523
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…





















