Tag it EASI – neue Methode zur genauen Proteinbestimmung

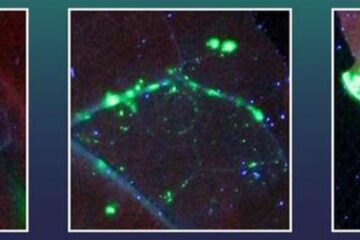
Ähnlich wie bei den Anhängern von Gepäckstücken vor einem Flug, werden Proteinproben für die Massenspektrometrie mit dem neuen EASI-tag markiert. © MPI für Biochemie
In den letzten Jahren haben Forscher erkannt, dass die Analyse der Gene, also der Erbinformation, nicht ausreicht, um zelluläre Prozesse in gesunden oder krankhaft veränderten Zellen zu verstehen. Denn es sind die Proteine, die unter anderem Aufgaben als Signalmoleküle, Regulatoren oder Strukturbausteine übernehmen.
Auf der Grundlage der Erbinformation, der Bauanleitung für Proteine, werden einzelne Aminosäuren zu Proteinen zusammengebaut. Während die Erbinformation in den verschiedenen Zellen eines Organismus gleich ist, ist die Proteinzusammensetzung in den verschiedenen Zelltypen unterschiedlich.
Massenspektrometrie zur Proteinanalyse
Deshalb konzentriert sich die Grundlagenforschung seit vielen Jahren auf die Analyse von Proteinen. Dafür nutzen die Forscher die Massenspektrometrie. Diese Methode erlaubt es, die Menge und die Art tausender Proteine in einer Probe, wie z.B. in Gewebe, zu bestimmen. Während diese Mess-methode in der Vergangenheit aufwendig war, ist es ein großes Ziel, das Verfahren für die klinische Diagnostik zu vereinfachen.
Diesem Ziel sind Forscher um Felix Meissner und Matthias Mann vom MPI für Biochemie wieder einen Schritt nähergekommen. Sie haben eine Markierungsmethode entwickelt, die es ermöglicht, verschiedene Proteinproben in einem Messansatz exakter als bisher zu messen.
„Bei vielen Fragestellungen wollen wir wissen, wie sich biologisches Material in seiner Proteinzusammensetzung unterscheidet. Das könnte der Vergleich zwischen Proben aus verschiedenen Geweberegionen sein oder von gesunden Personen und erkrankten Patienten“, erklärt Meissner. Hier ist es wichtig, dass die Proteinmengen so genau wie möglich bestimmt werden, denn zum Beispiel in der Medizin sind für die Diagnose von Erkrankungen häufig exakt definierte Grenzwerte entscheidend.
„Mit unserer neuen Methode können wir unterschiedliche Proteinmengen zwischen Proben viel genauer bestimmen, als mit altbekannten Verfahren“, so Meissner. Die zu vergleichenden Proben werden in einer Messung analysiert. „Dies reduziert die Zahl der Messungen, spart also Zeit und Geld und schließt technische Schwankungen aus, die bei aufeinander folgenden Messungen auftreten würden“, so Meissner weiter.
Die neue Markierung EASI-tag
Um die Proben voneinander zu unterscheiden, werden diese vor der Messung mit verschiedenen EASI-tag Molekülen markiert. „Das ist vergleichbar mit den Anhängern von Gepäckstücken vor einem Flug. Alle Gepäckstücke, so unterschiedlich sie sind, erhalten einen kleinen Anhänger. Im Flugzeug können alle Koffer gemischt sein, denn am Ende der Reise, ordnet das Flugpersonal jedes Gepäckstück anhand der Anhänger einer Person oder Reisegruppe zu. In unserem Fall können wir so Proteine einer bestimmten Probe zuordnen“, erklärt Meissner.
Während für eine Reise die Koffer mit Namensschildern versehen, ins Flugzeug verfrachtet, durch die Luft transportiert und nach der Landung wieder dem Eigentümer zugeordnet werden, gibt es auch in der massenspektrometrischen Analyse verschiedene aufeinanderfolgende Prozessschritte.
Anders als bei den Koffern im Flugzeug werden die vielen tausend Proteine erst enzymatisch zerkleinert und anschließend die entstandenen Proteinbruchstücke, die Peptide, mit verschiedenen EASI-tags markiert. Nun können unterschiedliche Proben gemischt und im Massespektrometer gemeinsam analysiert werden. Dabei fliegen die markierten Peptide durchs Massenspektrometer und werden gewogen.
„Zu diesem Zeitpunkt sind die Peptide noch keiner Probe zuzuordnen, denn die verschiedenen EASI-tags sind gleich schwer und unterscheiden sich nur durch die bestimmte Anordnung von schweren Kohlenstoffatomen“, erklärt Sebastian Virreira Winter, Erstautor der Studie.
Nun folgt ein zweiter Analyseschritt bei dem bestimmt wird, welche Peptide vorhanden sind und zu welcher Probe diese gehören. Um die Zusammensetzung der Peptide zu bestimmen werden diese durch Kollisionen zerbrochen und anschließend mit einer Datenbank aller möglichen menschlichen Peptidbruchstücke abgeglichen.
„Neben den Peptiden bricht auch der EASI-tag an einer definierten Sollbruchstelle. Die Bruchstücke von gleichen Peptiden aus verschiedenen Proben unterscheiden sich nun durch eine minimale Massendifferenz. Zum Beispiel trägt ein Peptid einer Probe einen „abgebrochenen“ EASI-tag mit zwei und das einer anderen Probe mit drei schweren Kohlenstoffatomen. „Jetzt haben wir die zu vergleichenden Signale der einzelnen Proben unmittelbar nebeneinander und können direkt und genau die Unterschiede messen.“ so Virreira Winter.
„Wenn wir bei der Analogie der Koffer bleiben wollen, sind diese am Ende des Fluges leider kaputt, aber wir wissen ganz genau, was drin war. Wir sind optimistisch, dass EASI-tag die Tür für viele Anwendungen, weiter öffnen wird, bei denen es auf genaue Proteinmengen ankommt. Wir würden uns freuen, wenn unsere Technologie z.B. Medizinern zukünftig exakte Analysen erlaubt, um präzise Diagnosen zu stellen“, fasst Meissner zusammen.
Originalpublikation
S.Virreira Winter*, F. Meier*, C. Wichmann, J. Cox, M. Mann and F. Meissner: EASI-tag enables accurate multiplexed and interference-free MS2-based proteome quantification, Nature Methods, Mai 2018 (*trugen zu gleichen Teilen bei)
—
Über Felix Meissner
Felix Meissner studierte Biochemie an der Freien Universität, Berlin und am Scripps Institute in San Diego, USA. Er promovierte 2008 am Max-Planck-Institut für Infektionsbiologie in Berlin. Seine Postdoktorandenzeit führte ihn dann weiter an das Max-Planck-Institut für Biochemie in Martinsried bei München, und die University of California in San Francisco, USA. Anschließend ging es als Gruppenleiter zurück nach München in die Abteilung „Proteomics und Signaltransduktion“ am MPI für Biochemie, geleitet von Matthias Mann. Seit 2015 leitet Meissner am selben Institut seine unabhängige Arbeitsgruppe „Experimentelle Systemimmunologie“.
Über das Max-Planck-Institut für Biochemie
Das Max-Planck-Institut für Biochemie (MPIB) in Martinsried bei München zählt zu den führenden internationalen Forschungseinrichtungen auf den Gebieten der Biochemie, Zell- und Strukturbiologie sowie der biomedizinischen Forschung und ist mit rund 35 wissenschaftlichen Abteilungen und Forschungsgruppen und ungefähr 800 Mitarbeitern eines der größten Institute der Max-Planck-Gesellschaft zur Förderung der Wissenschaften e.V. Das MPIB befindet sich auf dem Life-Science-Campus Martinsried in direkter Nachbarschaft zu dem Max-Planck-Institut für Neurobiologie, Instituten der Ludwig-Maximilians-Universität München und dem Innovations- und Gründerzentrum Biotechnologie (IZB). http://biochem.mpg.de
Kontakt:
Dr. Felix Meissner
Experimental Systems Immunology
Max Planck Institute of Biochemistry
Am Klopferspitz 18
82152 Martinsried/Munich
E-Mail: meissner@biochem.mpg.de
www.biochem.mpg.de/meissner
Dr. Christiane Menzfeld
Öffentlichkeitsarbeit
Max-Planck-Institut für Biochemie
Am Klopferspitz 18
82152 Martinsried
Tel. +49 89 8578-2824
E-Mail: pr@biochem.mpg.de
www.biochem.mpg.de
http://www.biochem.mpg.de/en – homepage max planck institute of biochemistry
http://www.biochem.mpg.de/meissner – homepage Felix Meissner
http://www.biochem.mpg.de/en/rd/mann – homepage Matthias Mann
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…
Durchbruch bei CRISPR/Cas
Optimierte Genschere erlaubt den stabilen Einbau von großen Genen. Großer Fortschritt an der CRISPR-Front. Wissenschaftlern des Leibniz-Instituts für Pflanzenbiochemie (IPB) ist es erstmals gelungen, sehr effizient große Gen-Abschnitte stabil und…

Rittal TX Colo: Das neue Rack für Colocation Data Center
Rittal TX Colo: Flexibel, skalierbar und zukunftssicher Mit der zunehmenden Digitalisierung und künftig auch immer mehr KI-Anwendungen steigt der Bedarf an Rechenleistung signifikant – und damit boomt der Colocation-Markt. Unternehmen…





















