Wenn Sauerstoff Proteinen zum Verhängnis wird
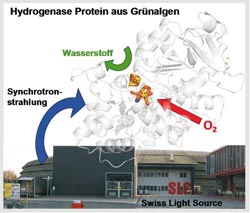
Mit der Swiss Light Source am Paul Scheerer-Institut in der Nähe von Zürich untersuchten Bochumer und Berliner Forscher das Hydrogenase-Protein, dessen dreidimensionale Struktur in der Abbildung zu sehen ist. Foto: Camilla Lambertz<br>
Warum Enzyme, die zur technischen Herstellung von Wasserstoff genutzt werden, so empfindlich gegenüber Sauerstoff sind, berichten Wissenschaftler der RUB-Fakultät für Biologie und Biotechnologie im Journal of Biological Chemistry.
Gemeinsam mit Berliner Forschern untersuchten sie mit spektroskopischen Methoden den Zeitverlauf der Vorgänge, die zur Inaktivierung der Enzymfunktion in so genannten Hydrogenasen führen. „Hydrogenasen könnten von herausragender Bedeutung sein, um Wasserstoff mit Hilfe von biologischen oder chemischen Katalysatoren zu gewinnen“, erklärt Camilla Lambertz aus der RUB-Arbeitsgruppe Photobiotechnologie. „Ihre hohe Sauerstoffempfindlichkeit stellt allerdings ein großes Problem dar. Unsere Ergebnisse können helfen, in Zukunft robustere Enzyme zu entwickeln.“
Sauerstoff als Freund und Feind
Für die meisten Tiere und Pflanzen ist Sauerstoff überlebensnotwendig, doch wirkt er in zu hohen Konzentrationen auf viele Lebewesen giftig und einige Organismen können sogar nur ganz ohne Sauerstoff existieren. Die Sensibilität gegenüber Sauerstoff findet man auch auf der Ebene der Proteine. So ist eine Vielzahl von Enzymen, z.B. Hydrogenasen, bekannt, die durch Sauerstoff irreversibel zerstört werden. Hydrogenasen sind biologische Katalysatoren, die Protonen und Elektronen in technisch nutzbaren Wasserstoff umwandeln. Das RUB-Team um Prof. Dr. Thomas Happe erforscht sogenannte [FeFe]-Hydrogenasen, die besonders viel Wasserstoff produzieren können. Die Bildung von Wasserstoff findet u.a. an zwei speziellen Eisenatomen des Enzyms statt, die gemeinsam mit anderen Atomen das reaktive Zentrum formen.
Sauerstoff greift Eisenzentren an
Gemeinsam mit der Arbeitsgruppe von Dr. Michael Haumann in Berlin fanden die Forscher heraus, dass Sauerstoff sich an das Zweieisenzentrum der Hydrogenase bindet und dadurch einen anderen Bereich des Enzyms aus vier weiteren Eisenatomen ausschaltet. In dem vom BMBF geförderten Forschungsprojekt zeigten sie erstmals die verschiedenen Phasen des Inaktivierungsprozesses mit der so genannten Röntgenabsorptionsspektroskopie. Für die spezielle Art der Messung nutzen die Wissenschaftler die Synchrotronstrahlungsquelle Swiss Light Source in der Schweiz, die besonders starke Röntgenstrahlen erzeugt und somit die Charakterisierung von Metallzentren in Proteinen erlaubt. So bestimmten die Forscher unter anderem die chemische Natur der Eisenzentren und den Abstand zu den Nachbaratomen mit atomarer Auflösung.
Inaktivierung in drei Stufen
Das Team der Bochumer und Berliner Wissenschaftler setzte ein neues experimentelles Protokoll ein. Sie brachten die Hydrogenaseproben erst für einige Sekunden bis Minuten und zuletzt für einige Stunden mit Sauerstoff in Kontakt und unterbanden dann alle weiteren Reaktionen durch Tiefgefrieren in flüssigem Stickstoff. Aus den anschließend gewonnenen spektroskopischen Daten erstellten sie ein Modell für einen dreistufigen Prozess der Inaktivierung. Laut Modell bindet zunächst ein Sauerstoffmolekül an das Zweieisenzentrum der Hydrogenase, woraufhin eine aggressive Sauerstoffspezies entsteht. Diese greift in der folgenden Phase das Viereisenzentrum an und modifiziert es. Im letzten Schritt binden weitere Sauerstoffmoleküle und der gesamte Komplex zerfällt. „Der ganze Vorgang beinhaltet also mehrere aufeinanderfolgende Reaktionen, die zeitlich klar getrennt auftreten“, so Lambertz. „Die Geschwindigkeit des Gesamtprozesses wird möglicherweise durch den Schritt bestimmt, in dem die aggressive Sauerstoffspezies vom Zwei- zum Viereisenzentrum wandert. Wir bereiten gerade weitere Experimente vor, um das zu prüfen.“
Titelaufnahme
C. Lambertz, N. Leidel, K.G.V. Havelius, J. Noth, P. Chernev, M. Winkler, T. Happe, M. Haumann (2011) O2-reactions at the six-iron active site (H-cluster) in [FeFe]-hydrogenase, Journal of Biological Chemistry, doi: 10.1074/jbc.M111.283648
Weitere Informationen
Camilla Lambertz, Arbeitsgruppe Photobiotechnologie, Fakultät für Biologie und Biotechnologie der Ruhr-Universität, 44780 Bochum, Tel.: 0234/32-24496
Camilla.Lambertz@rub.de
Thomas Happe, Arbeitsgruppe Photobiotechnologie, Fakultät für Biologie und Biotechnologie der Ruhr-Universität, 44780 Bochum, Tel.: 0234/32-27026
Thomas.Happe@rub.de
Redaktion: Dr. Julia Weiler
Media Contact
Weitere Informationen:
http://www.ruhr-uni-bochum.de/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















