Positionsbestimmung von Muskelproteinen
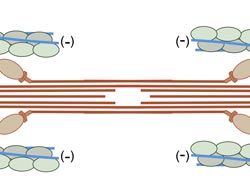
Schematische Zeichnung des Sarkomers. Die Z-Scheibe ist in schwarz dargestellt, Aktin in grün/grau , Tropomyosin in blau und Myosin in rot.<br> © MPI für molekulare Physiologie <br>
Muskelkontraktion und viele andere Bewegungsprozesse werden durch das Zusammenspiel zwischen Myosin- und Aktinfilamenten gesteuert. Zwei weitere Proteine, Tropomyosin und Troponin regulieren die Bindung des Myosins an Aktin.
Wie genau diese Muskelproteine interagieren, ist zwar in theoretischen Modellen beschrieben, allerdings bisher nie im Detail beobachtet worden. Stefan Raunser und Elmar Behrmann vom Max-Planck-Institut für molekulare Physiologie in Dortmund ist es nun gelungen, den Aktin-Myosin-Tropomyosin-Komplex mit bisher unerreichter Genauigkeit von 0.8 Nanometern sichtbar zu machen – was einer Auflösung von weniger als einem Millionstel Millimeter entspricht. Dies ermöglicht es erstmals, die Proteine innerhalb des Komplexes korrekt zu positionieren und die Vorgänge bei der Muskelkontraktion zu analysieren. Mit diesen Erkenntnissen könnte aufgeklärt werden, wie sich genetisch bedingte Veränderungen des Aktin-Myosin-Tropomyosin-Komplexes auf manche vererbbare Herzerkrankungen auswirken.
Die zentrale funktionelle Einheit, das Sarkomer, eines Muskels besteht aus Aktin-, Myosin- und Tropomyosin-Proteinen. Damit sich ein Muskel zusammenziehen kann, muss das Myosin an den fadenförmigen Aktinmolekülen entlang gleiten. Zusammen mit Troponin reguliert Tropomyosin die Muskelkontraktion, indem es steuert wann Myosin an Aktin gebunden ist. Im Ruhezustand blockieren Tropomyosin und Troponin die Bindungsstelle für Myosin am Aktinfilament. Der Myosinkopf befindet sich dann in 90 Grad Stellung. Erst durch einströmendes Calcium, das an die Regulationsproteine andockt, wird die Bindungsstelle am Aktinfilament frei gelegt. Der Myosinkopf dockt an diese an, ändert seine Konformation und knickt gelenkartig ab, wobei er das Aktin mit sich zieht. Das aneinander Vorbeigleiten der Filamente führt zu einer Verkürzung des Sarkomers und somit zum Zusammenziehen des Muskels.
Die diesem Modell zugrundeliegende Wechselwirkung zwischen Aktin, Myosin und Tropomyosin konnten Wissenschaftler des Max-Planck-Instituts für molekulare Physiologie in Zusammenarbeit mit Wissenschaftlern der Medizinischen Hochschule Hannover, der Ruhr-Uni Bochum und der University of Texas in Houston, nun erstmals im Detail zeigen. Dank der verbesserten technischen Möglichkeiten im Bereich der Elektronenmikroskopie erhalten Stefan Raunser und seine Kollegen erstmals einen genauen Einblick in die strukturellen Elemente des Muskels. „Ein wichtiger Schritt um das Zusammenspiel der einzelnen Proteine innerhalb der funktionellen Strukturen des Muskels zu verstehen“, sagt Raunser.
So bestimmten sie beispielsweise die genaue Position von Tropomyosin auf dem Aktin-Filament im Myosin-gebundenen Zustand und zeigten durch die im Detail sichtbar gemachte Struktur des Komplexes, dass Aktin tatsächlich Konformationsänderungen in Myosin bewirkt. Vergleiche mit Moysinstrukturen in anderen Zuständen ermöglichen es den Forschern, das Zusammenspiel von Myosin und Aktin während der Muskelkontraktion zu beschreiben. „Wir haben so etwas wie eine Landkarte für Biochemiker gebastelt. Für sie wird es durch unsere Ergebnisse künftig leichter Prozesse und Abläufe innerhalb der Muskulatur zu verstehen“, so Raunser.
Darüber hinaus sind die Ergebnisse aus medizinischer Sicht von hoher Relevanz. Das menschliche Herz ist der wichtigste Muskel im menschlichen Körper, funktioniert er nicht optimal, so kann dies zum Tod führen. Fehlfunktionen innerhalb des Herzens hängen oft mit Punktmutationen zusammen. Die Aufnahmen der Max-Planck-Forscher ermöglichen nun erstmals diese Mutationen genau zu positionieren. „Die genaue Position der Mutationen zu erkennen ist eine Grundvoraussetzung um Therapien für solche Herzerkrankungen zu entwickeln“, sagt Stefan Raunser.
Ansprechpartner
Dr. Stefan Raunser
Max-Planck-Institut für molekulare Physiologie
Telefon: +49 231 133-2356
Email: stefan.raunser@mpi-dortmund.mpg.de
Dr. Peter Herter
Max-Planck-Institut für molekulare Physiologie
Telefon: +49 231 133-2500
Fax: +49 231 133-2599
Email: peter.herter@mpi-dortmund.mpg.de
Originalveröffentlichung
Behrmann, Müller, Penczek, Mannherz, Manstein und Raunser
Structure of the Rigor Actin-Tropomyosin-Myosin Complex
Cell,20 July 2012
Media Contact
Weitere Informationen:
http://www.mpg.de/5897741/MuskelkontraktionAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















