Horch her! Wie sich Nervenzellen akustischen Signalen flexibel anpassen
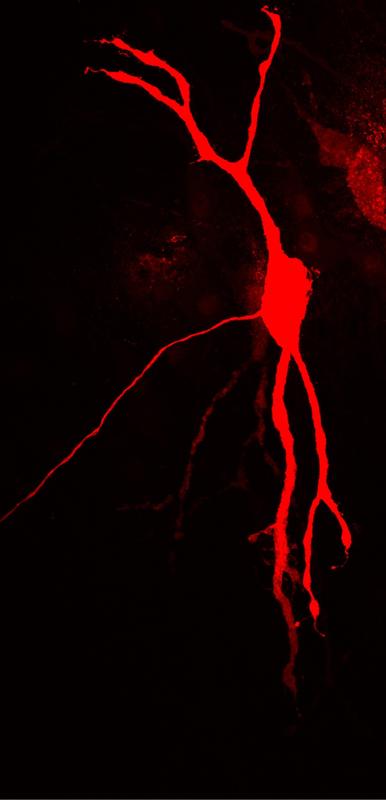
Eine Nervenzelle im Hirnstamm, die akustische Informationen verarbeitet. Je nach Situation lässt sie die Aktionspotentiale am Axon (dünner Fortsatz links) nah oder entfernt vom Zellkörper entstehen. Felix Felmy, 2014
Um akustische Informationen mit hoher zeitlicher Präzision zu verarbeiten, könnten Nervenzellen ihre Arbeitsweise flexibel der Situation anpassen. Bei geringer Frequenz der Eingangssignale erzeugen sie die meisten ausgehenden Aktionspotentiale nah am Zellkörper.
Nach hemmenden oder hochfrequenten Signalen hingegen lassen die Zellen viele Aktionspotentiale weiter entfernt entstehen. So sind sie maximal empfänglich für die unterschiedlichsten Arten von Eingangssignalen.
Zu dieser Erkenntnis ist ein Team von Wissenschaftlern um Professor Christian Leibold, Professor Benedikt Grothe und Dr. Felix Felmy vom Bernstein Zentrum und dem Bernstein Fokus Neurotechnologie in München, sowie der Ludwig-Maximilians-Universität München mithilfe von Computermodellen gekommen. Die Forscher berichten in der neusten Ausgabe der Zeitschrift Journal of Neuroscience über ihre Ergebnisse.
Kam der Knall von vorne oder von rechts? Um Schallquellen zu lokalisieren, werten Nervenzellen im Hirnstamm die Unterschiede der Ankunftszeit des Signals an beiden Ohren aus. Sie können dazu Differenzen von bis zu zehn millionstel Sekunden detektieren. Diese Fähigkeit verlangt, dass die Neurone sehr schnell erregt werden.
Dabei ändern sie die elektrische Spannung, die über ihre Zellmembran herrscht. Wird ein bestimmter Schwellenwert überschritten, generieren Nervenzellen ein starkes elektrisches Signal – ein sogenanntes Aktionspotential – welches effizient über die weite Strecke ihres Axons weitergeleitet werden kann ohne abgeschwächt zu werden Um den Schwellenwert zu überschreiten werden erregende Eingangssignale aufsummiert. Dies gelingt besser, je langsamer die Nervenzellen die elektrische Spannung über ihren Zellmembranen ändern.
Diese beide Anforderungen – schnelle Spannungsänderungen für eine hohe zeitliche Auflösung der Eingangssignale und langsame Spannungsänderungen für eine optimale Integration der Signale zur Erzeugung eines Aktionspotentials – stellen die Nervenzelle vor eine paradoxe Herausforderung. „Die Natur löst dieses Problem, indem sie beide Vorgänge räumlich trennt: die Eingangssignale werden im Zellkörper und den Dendriten verarbeitet, Aktionspotentiale entstehen im Zellfortsatz, dem Axon“, erklärt Leibold, Leiter der Studie. Doch wie nachhaltig ist diese räumliche Trennung?
In ihrer Studie maßen die Forscher die Geometrie des Axons und den Schwellenwert der entsprechenden Zellen und konstruierten damit ein Computermodell, mit dem sie die Effizienz dieser örtlichen Trennung untersuchten. Das Modell der Wissenschaftler sagt voraus, dass Neurone je nach Situation Aktionspotentiale mehr oder weniger nah am Zellkörper bilden.
Bei hochfrequenten oder hemmenden Eingangssignalen verlagern sie deren Entstehungsort von der Ursprungsstelle des Axons vorzugsweise in weiter entfernte Bereiche. Auf diese Weise stellen die Zellen sicher, dass sie Eingangssignale unterschiedlichster Art optimal verarbeiten – und wir dadurch sowohl kleine als auch große zeitliche Schalldifferenzen gut wahrnehmen und Geräusche im Raum orten können.
Das Bernstein Zentrum München ist Teil des Nationalen Bernstein Netzwerks Computational Neuroscience. Seit 2004 fördert das Bundesministerium für Bildung und Forschung (BMBF) mit dieser Initiative die neue Forschungsdisziplin Computational Neuroscience mit über 170 Mio. €. Das Netzwerk ist benannt nach dem deutschen Physiologen Julius Bernstein (1835-1917).
Weitere Informationen erteilen Ihnen gerne:
Prof. Dr. Christian Leibold
Computational Neuroscience
Department Biology II
Ludwig-Maximilians-Universität München
Großhaderner Straße 2
82152 Planegg-Martinsried
Tel: +49 (0)89 2180-74802
Email: leibold@bio.lmu.de
Originalpublikation:
S. Lehnert, M. C. Ford, O. Alexandrova, F. Hellmundth, F. Felmy, B. Grothe & C. Leibold (2014): Action potential generation in an anatomically constrained model of medial superior olive axons. Journal of Neuroscience, 34(15): 5370—5384.
http://neuro.bio.lmu.de/research_groups/res-leibold_ch persönliche Webseite Christian Leibold
http://www.bccn-munich.de Bernstein Zentrum München
http://www.uni-muenchen.de Ludwig-Maximilians-Universität München
http://www.nncn.de Nationales Bernstein Netzwerk Computational Neuroscience
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Neue universelle lichtbasierte Technik zur Kontrolle der Talpolarisation
Ein internationales Forscherteam berichtet in Nature über eine neue Methode, mit der zum ersten Mal die Talpolarisation in zentrosymmetrischen Bulk-Materialien auf eine nicht materialspezifische Weise erreicht wird. Diese „universelle Technik“…

Tumorzellen hebeln das Immunsystem früh aus
Neu entdeckter Mechanismus könnte Krebs-Immuntherapien deutlich verbessern. Tumore verhindern aktiv, dass sich Immunantworten durch sogenannte zytotoxische T-Zellen bilden, die den Krebs bekämpfen könnten. Wie das genau geschieht, beschreiben jetzt erstmals…

Immunzellen in den Startlöchern: „Allzeit bereit“ ist harte Arbeit
Wenn Krankheitserreger in den Körper eindringen, muss das Immunsystem sofort reagieren und eine Infektion verhindern oder eindämmen. Doch wie halten sich unsere Abwehrzellen bereit, wenn kein Angreifer in Sicht ist?…





















