Fastenzeit für Tumorzellen
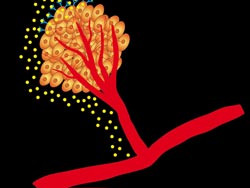
Positive Rückkoplung: Krebszellen schütten das Hormon VEGF (gelb) aus und stimulieren so Blutgefäße in der Nähe (rot) zur Ausbildung kleiner Fortsätze. Gleichzeitig bilden sie außerdem VEGF-Rezeptoren-2 (blau), an denen sich das VEGF bindet. Dadurch werden die Krebszellen angeregt, noch mehr VEGF zu produzieren.<br>© MPI für neurologische Forschung<br>
Tumore müssen mit ausreichend Nährstoffen versorgt werden, um wachsen zu können. Um die Nährstoffversorgung sicherzustellen, regen sie benachbarte Blutgefäße mithilfe von Botenstoffen zur Sprossung an.
Wissenschaftler vom Max-Planck-Institut für neurologische Forschung in Köln haben nun eine neue positive Rückkopplungsschleife des Hormons VEGF identifiziert, über die VEGF durch Bindung an den VEGF-Rezeptor-2 auf den Krebszellen seine eigene Ausschüttung ankurbelt und so das Tumorwachstum beschleunigt. In Versuchen an Mäusen mit Lungenkrebs schalteten sie die zuständigen Hormone aus und verlangsamten so das Wachstum der Tumore.
In Kombination mit anderen Hemmstoffen schrumpften sie sogar. Damit haben die Forscher die Existenz des VEGF-Rezeptors-2 auf Tumorzellen bewiesen und einen neuen Signalweg in Tumorzellen beschrieben, der die Ausbildung neuer Blutgefäße auslöst. Durch Untersuchungen an Lungenkrebspatienten haben sie zudem herausgefunden, dass eine Therapie mit solchen Hemmstoffen nur dann sinnvoll ist, wenn die Krebszellen besonders viele VEGF-Rezeptoren 2 ausbilden. Die Ergebnisse könnten dazu beitragen, neue Krebstherapien zu entwickeln.
Bevor Tumorzellen sich unkontrolliert teilen, verharren sie oft in einer Art Ruhezustand. Dabei sterben etwa immer genauso viele Zellen ab wie sich neubilden. Erst eine Veränderung im Erbgut führt dazu, dass Botenstoffe gebildet werden, die das Wachstum von Blutgefäßen anregen. Erst dann kann der Tumor anfangen zu wachsen. Ohne diesen Übergang vom ruhenden in den aktiven Zustand wäre das Wachstum der Krebszellen auf eine für den Körper ungefährliche Größe beschränkt.
Wissenschaftler am Max-Planck Institut für neurologische Forschung wollen dies als Angriffspunkt in der Tumortherapie nutzen. Dafür haben sie die Wirkung von VEGF untersucht, das Blutgefäße auswachsen lässt. Den Wissenschaftlern um Roland Ullrich zufolge wirkt VEGF auch direkt auf die ausschüttenden Tumorzellen ein. Diese nehmen es wieder über Rezeptoren auf und produzieren so noch mehr VEGF. „Diese positive Rückkopplungsschleife sorgt dafür, dass sich immer mehr Blutgefäße ausbilden und der Krebs dadurch noch schneller wächst“, erklärt Ullrich. „Wir wollten deshalb herausfinden, was passiert wenn wir sie unterbrechen.“ Die Idee der Wissenschaftler: Den Krebs von der Nährstoffzufuhr abzuschneiden – ihn einfach auszuhungern. Ullrich vergleicht den Kampf gegen den Krebs mit der Belagerung einer Festung: „Man muss die Burg nicht unbedingt erstürmen, um den Gegner zu bezwingen. Es genügt, den Wasserhahn zuzudrehen.“
Im zweiten Teil ihrer Studie untersuchten sie deshalb Mäuse die eine bestimmte Form von Lungenkrebs aufwiesen und blockierten den VEGF-Rezeptor 2. „Und tatsächlich stellten wir bei den Tieren eine Verlangsamung des Krebswachstums fest“, sagt Ullrich. „Noch beeindruckender war das Ergebnis, wenn wir einen weiteren Hemmer hinzugaben.“ Dieser stört den sogenannten MAPK-Signalweg, der unter anderem das Wachstum der Tumorzellen antreibt. Einzeln gegeben zögerten die beiden Inhibitoren das Krebswachstum nur hinaus, in Kombination allerdings ließen sie den Krebs tatsächlich schrumpfen. Die Wissenschaftler vermuten deshalb, dass es einen Zusammenhang zwischen der Hemmung des VEGF-Rezeptor 2 und dem MAPK-Signalweg gibt. „Wird den Zellen die Nährstoffzufuhr abgeschnitten, fangen diese einfach an stärker zu wachsen“, erklärt Ullrich. „Und das können wir mit Hilfe des zweiten Hemmers verhindern.“
Doch nicht alle Krebstypen sind für eine solche Behandlung geeignet. Denn nur wenn die Krebszellen auch die Rezeptoren für VEGF auf ihrer Membran ausbilden, können die Hemmstoffe überhaupt wirksam werden. Den Ergebnissen der Kölner Wissenschaftler zufolge besitzt etwa jeder fünfte Lungenkrebspatient VEGF-Rezeptoren-2 auf den Krebszellen und könnte folglich auf diese Weise behandelt werden.
Ansprechpartner
Dr Roland Ullrich,
Max-Planck-Institut für neurologische Forschung, Köln
Telefon: +49 221 4726-226
E-Mail: ullrich@nf.mpg.de
Caroline Wieczorek,
Max-Planck-Institut für neurologische Forschung, Köln
E-Mail: Caroline.Wieczorek@nf.mpg.de
Originalpublikation
Sampurna Chatterjee, Lukas C. Heukamp, Maike Siobal, Jakob Schöttle, Caroline Wieczorek, Martin Peifer, Davide Frasca, Mirjam Koker, Katharina König, Lydia Meder, Daniel Rauh, Reinhard Buettner, Jürgen Wolf, Rolf A. Brekken, Bernd Neumaier, Gerhard Christofori, Roman K. Thomas, and Roland T. Ullrich
Tumor VEGF:VEGFR2 autocrine feed-forward loop triggers angiogenesis in lung cancer
J Clin Invest. 2013;123(4) doi:10.1172/JCI65385
Media Contact
Weitere Informationen:
http://www.mpg.de/6995353/Fastenzeit_fuer_tumorzellenAlle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Bakterien für klimaneutrale Chemikalien der Zukunft
Forschende an der ETH Zürich haben Bakterien im Labor so herangezüchtet, dass sie Methanol effizient verwerten können. Jetzt lässt sich der Stoffwechsel dieser Bakterien anzapfen, um wertvolle Produkte herzustellen, die…

Batterien: Heute die Materialien von morgen modellieren
Welche Faktoren bestimmen, wie schnell sich eine Batterie laden lässt? Dieser und weiteren Fragen gehen Forschende am Karlsruher Institut für Technologie (KIT) mit computergestützten Simulationen nach. Mikrostrukturmodelle tragen dazu bei,…

Porosität von Sedimentgestein mit Neutronen untersucht
Forschung am FRM II zu geologischen Lagerstätten. Dauerhafte unterirdische Lagerung von CO2 Poren so klein wie Bakterien Porenmessung mit Neutronen auf den Nanometer genau Ob Sedimentgesteine fossile Kohlenwasserstoffe speichern können…





















