Demenz in der Petrischale
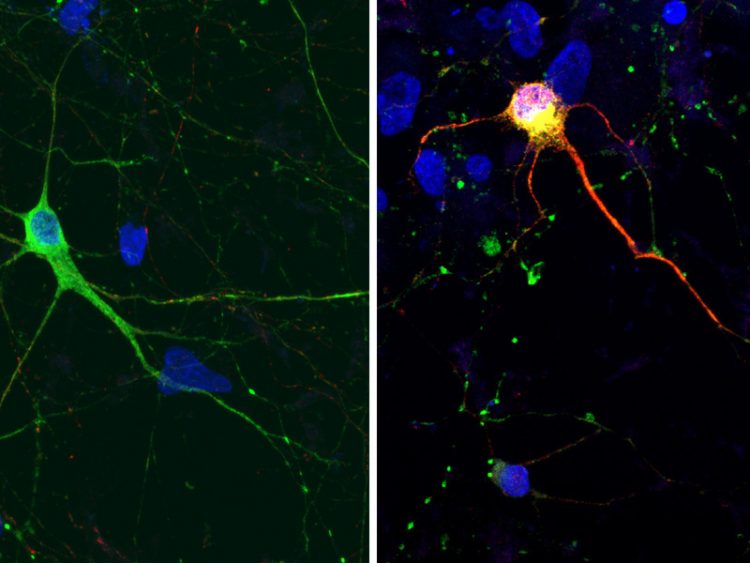
Nervenzellen, abgeleitet von iPS-Zellen von einer gesunden Person (links) und einem Patienten mit einer FTD-assoziierten Tau-Mutation (rechts). In Grün angefärbt ist ein Marker für Nervenzellen. Die rote Farbe zeigt krankhaft verändertes Tau-Protein. Die gelb/orangene Farbe entsteht durch Überlagerung der beiden Färbungen. In Blau sind Zellkerne dargestellt. © MPI für molekulare Biomedizin / A.-L. Hallmann
Die Frontotemporale Demenz (FTD) ist eine neurodegenerative Erkrankung, bei der im Stirn- und Schläfenbereich (Fronto-Temporal-Lappen) des Gehirns Nervenzellen absterben. Allein in Deutschland sind etwa 33.000 Menschen von dieser Krankheit betroffen, wobei die genauen Mechanismen für die Neurodegeneration bislang nicht bekannt sind.
Es gibt daher keine Therapie, mit der die FTD geheilt oder gestoppt werden könnte. Wissenschaftler der Medizinischen Fakultät der Universität Münster und des Max-Planck-Instituts für molekulare Biomedizin haben nun mithilfe induzierter pluripotenter Stammzellen (iPS) ein Krankheitsmodell der FTD in der Kulturschale entwickelt.
Mit dieser Technik ist es ihnen gelungen, ein Gen zu identifizieren, das in den erkrankten Nervenzellen eine schützende Rolle hat. Darüber hinaus zeigten die Wissenschaftler, dass die FTD-iPS-Zellen für Medikamentenscreenings genutzt werden könnten, um möglicherweise eine Therapie für FTD zu entwickeln.
Die Frontotemporale Demenz (FTD) ist tückisch: Erste Symptome sind Veränderungen der Persönlichkeit und des zwischenmenschlichen Verhaltens – Veränderungen, die anfangs leicht mit einer depressiven Verstimmung oder einem Burn-out-Syndrom abgetan werden können. Erst wenn sich später Störungen der Sprache und des Gedächtnisses entwickeln, wird oft die umfassende Diagnose gestellt. Meistens erkranken Patienten zwischen dem 50. und 60. Lebensjahr; bei der erblichen Form treten erste Symptome schon zwischen 40 und 50 Jahren auf. Die Krankheit schreitet dann schnell fort und kann innerhalb von 5 bis 10 Jahren zum Tod führen.
FTD ist eine neurodegenerative Erkrankung, bei der es, wie bei Alzheimer, in vielen Patienten zu Ablagerungen des sogenannten Tau-Proteins in verschiedenen Hirnregionen kommt. Dieses Protein existiert in Nervenzellen und ist wichtig für die mechanische Stabilität der Zellen sowie für Bewegungen und Transporte innerhalb der Zelle. In vielen FTD-Patienten wird das Tau-Protein übermäßig mit Phosphatgruppen beladen, und es kommt zu Verklumpung dieser veränderten Tau-Proteine.
Dadurch können in der Zelle Stabilisierungs- und Transportprozesse gestört werden, was letztlich zu ihrem Absterben führt. Ungefähr 20 bis 30 Prozent der FTD-Patienten haben eine erbliche Form der Krankheit, bei etwa 15 bis 20 Prozent dieser Patienten ist das Gen, das für das Protein Tau kodiert, verändert.
Diese Mutation bei der erblichen Form von FTD haben sich Wissenschaftler der Medizinischen Fakultät der Universität Münster und des Max-Planck-Instituts (MPI) für molekulare Biomedizin zunutze gemacht, um die Krankheit mithilfe der iPS-Technologie in die Kulturschale zu bringen.
„Die Erforschung der Mechanismen zur Entstehung der Frontotemporalen Demenz war bisher stark eingeschränkt, da die notwendigen betroffenen Nervenzellen nur in sehr geringen Umfang und dann auch meist in einem Endstadium der Erkrankung zur Verfügung stehen. Unser Team hat am MPI Hautzellen von Patienten mit FTD-assoziierten Tau-Mutationen zu induziert pluripotenten Stammzellen (iPS) reprogrammiert, wodurch es uns möglich war, die betroffenen Nervenzellen in der Zellkulturschale in praktisch unbegrenzten Mengen herzustellen,“ sagt Gunnar Hargus, Arzt am Institut für Neuropathologie des Universitätsklinikums Münster, der gemeinsam mit Professorin Tanja Kuhlmann, Ärztin am selben Institut, und Jared Sterneckert, Arbeitsgruppenleiter am MPI (jetzt Center for Regenerative Therapies Dresden), die Studie betreut hat.
Der große Vorteil der hier verwendeten iPS-Zellen ist, dass diese sich praktisch in jeden Zelltyp des menschlichen Körpers entwickeln können. Dadurch ist man nicht mehr auf die seltenen Patientenproben angewiesen, sondern kann die für die Erforschung einer Krankheit benötigten betroffenen Zellen in beliebiger Anzahl herstellen.
„In verschiedenen Tests haben wir zeigen können, dass die aus iPS-Zellen abgeleiteten Nervenzellen mit einer Tau-Mutation unter anderem kürzere Fortsätze haben und sich als Modell für die Suche nach neuen Therapien bzw. Wirkstoffen eignen,“ sagt Marc Ehrlich, Doktorand des Instituts für Neuropathologie und Erstautor der Studie. „Dieses Zellmodell könnte darüber hinaus auch für die Therapie anderer neurodegenerativer Erkrankungen eine große Bedeutung haben.“
Die Forscher zeigten unter anderem, dass die Nervenzellen mit einer Tau-Mutation unter simulierten Stressbedingungen schneller absterben als Nervenzellen ohne eine Tau-Mutation. Durch den Einsatz bestimmter Substanzen konnte der stressbedingte Zelltod in den erkrankten Nervenzellen rückgängig gemacht werden.
Um eine Idee zu bekommen, was auf molekularer Ebene in erkrankten Zellen passiert, schauten sich die Wissenschaftler das Genprofil an. Ein Gen sprang den Forschern quasi besonders ins Auge: „Unter all den Genen, die in erkrankten Zellen hochreguliert waren, haben wir ein Gen identifiziert, das eine schützende Rolle in den erkrankten Nervenzellen hat,“ sagt Anna-Lena Hallmann. Hallmann ist Ko-Erstautorin der Studie und ebenfalls Doktorandin am Institut für Neuropathologie. „Auch in Gewebeproben von verstorbenen Patienten konnten wir nachweisen, dass dieses Gen mit dem Namen MAGEH1 vermehrt abgelesen wird,“ sagt Hallmann.
„Völlig neu ist, dass wir MAGEH1 in einen Zusammenhang mit FTD gebracht haben“, sagt Ehrlich. „Als wir das Gen in den aus Tau-iPS-Zellen abgeleiteten Nervenzellen künstlich drosselten, ging es den Zellen schlechter; als wir es in gesunden Nervenzellen anregten, konnten sie sich besser gegen Stress wehren.“ „Tau-iPS-Zellen eignen sich also sehr gut als Modell für FTD, um molekulare Mechanismen der Krankheit besser als bisher zu untersuchen. Zudem könnte das Gen MAGEH1 eine sehr wichtige Rolle bei der Entwicklung neuer Therapieoptionen der FTD spielen,“ sagt Hallmann.
Ansprechpartner
Dr. Gunnar Hargus
Institut für Neuropathologie
Max-Planck-Institut für molekulare Biomedizin, Münster
E-Mail: gunnar.hargus@mpi-muenster.mpg.de
Dr. Jeanine Müller-Keuker
PR-Referentin
Max-Planck-Institut für molekulare Biomedizin, Münster
Telefon: +49 251 70365-325
E-Mail: j.mueller-keuker@mpi-muenster.mpg.de
Dr. Thomas Bauer
GB Unternehmenskommunikation
Universitätsklinikum Münster
Telefon: +49 251 83-58937
E-Mail: thbauer@uni-muenster.de
Originalpublikation
Marc Ehrlich, Anna-Lena Hallmann, Peter Reinhardt, Marcos J. Araúzo-Bravo, Sabrina Korr, Albrecht Röpke, Olympia E. Psathaki, Petra Ehling, Sven G. Meuth, Adrian L. Oblak, Jill R. Murrell, Bernardino Ghetti, Holm Zaehres, Hans R. Schöler, Jared Sterneckert, Tanja Kuhlmann, Gunnar Hargus
Distinct neurodegenerative changes in an induced pluripotent stem cell model of frontotemporal dementia linked to mutant TAU protein
Stem Cell Reports, online vorab 02. Juli 2015, doi:10.1016/j.stemcr.2015.06.001
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Erstmals 6G-Mobilfunk in Alpen getestet
Forschende der Universität Stuttgart erzielen leistungsstärkste Verbindung. Notrufe selbst in entlegenen Gegenden absetzen und dabei hohe Datenmengen in Echtzeit übertragen? Das soll möglich werden mit der sechsten Mobilfunkgeneration – kurz…

Neues Sensornetzwerk registriert ungewöhnliches Schwarmbeben im Vogtland
Das soeben fertig installierte Überwachungsnetz aus seismischen Sensoren in Bohrlöchern zeichnete Tausende Erdbebensignale auf – ein einzigartiger Datensatz zur Erforschung der Ursache von Schwarmbeben. Seit dem 20. März registriert ein…

Bestandsmanagement optimieren
Crateflow ermöglicht präzise KI-basierte Nachfrageprognosen. Eine zentrale Herausforderung für Unternehmen liegt darin, Über- und Unterbestände zu kontrollieren und Lieferketten störungsresistent zu gestalten. Dabei helfen Nachfrage-Prognosen, die Faktoren wie Lagerbestände, Bestellmengen,…