Biologie-orientierte Synthese (BIOS):Vom Naturstoff zu neuen Therapeutika
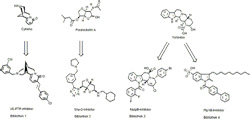
Entwicklung von Phosphatase-Inhibitoren durch die synergistische Anwendung der "Biologie-Orientierten Synthese" (BIOS) und der Klassifizierung der Substanzen in baumartigen Strukturen (SCONP). Die Naturstoffe Cytisin und Furanodictin A wurden hierbei derart modifiziert, dass sie die Enzyme VE-PTP und Shp-2 im niedrigen, mikromolaren Bereich hemmen. Ausgehend vom komplexen Naturstoff Yohimbin wurden mit Hilfe des SCONP-Prinzips (s. auch Abb. 2) das Indolochinolizidin- und das Indol-Grundgerüst als Ausgangspunkte für die Bibliotheken 3 und 4 ausgewählt, die wiederum zu nanomolaren Inhibitoren der Phosphatase MptpB sowie zu Hemmstoffen von Ptp1B in niederen, mikromolaren Bereich geführt haben. Bild: Max-Planck-Institut für molekulare Physiologie
Phosphatasen sind Schlüsselregulatoren zahlreicher Lebensprozesse und deshalb wichtiges Ziel zahlreicher Programme zur Wirkstoffsuche, etwa in der Diabetes- und der Antikrebs-Forschung. Doch noch steckt die Kenntnis über diese Enzyme in den Kinderschuhen, neue Inhibitoren für ihre Aktivität werden daher dringend gesucht. Jetzt ist es Wissenschaftlern des Max-Planck-Instituts für molekulare Physiologie in Dortmund mit dem von ihnen entwickelten Prinzip der "Biologie-orientierten Synthese (BIOS)" gelungen, vier völlig unbekannte Klassen von Phosphatase-Inhibitoren auf einmal zu entdecken. Damit eröffnen sich neue Wege zur Erforschung dieser Enzyme, die auch zu neuen Substanz-Kandidaten für die Wirkstoffforschung führen können (PNAS, Early Edition, 26. – 30. Juni 2006).
Naturstoffe sind- als in lebenden Organismen erprobte Ausgangspunkte- sehr gut geeignet für die Suche nach neuen Therapeutika. Naturstoffe entstehen durch Biosynthese und stellen somit durch die Evolution ausgewählte, chemische Strukturen dar, deren strukturelle Eigenschaften an ihre jeweilige Funktion angepasst wurden, die meist durch Interaktion mit verschiedenen Proteinen vermittelt wird.
Bei dem Prinzip der "Biologie-Orientierten Synthese" (BIOS) dienen Naturstoffe als Startpunkte für die Suche nach neuen Wirkstoffen. Um die Naturstoffe an das jeweilige Enzym anzupassen, werden chemische Reste nach dem Abbild der Natur entweder in Bereichen biologischer Relevanz eingeführt (Naturstoff-abgeleitete Synthese) oder man nutzt in der "Naturstoff-inspirierten Synthese" nicht den Naturstoff selbst, sondern nur einige seiner relevanten Kernstrukturen.
Wie wirksam dieses Prinzips ist, haben die Dortmunder Max-Planck-Forscher nun anhand von Phosphatasen belegt. Phosphatasen sind Enzyme, die Tyrosin- oder Serinreste in Enzymen dephosphorylieren. Obwohl diese Enzymklasse in den vergangenen Jahren durch die Krebs- und Diabetesforschung vermehrt in den Fokus der Pharmaforschung gerückt ist, ist das Wissen über Phosphatasen noch völlig ungenügend. Um neue Phosphataseinhibitor-Klassen mit Hilfe des BIOS-Konzepts zu identifizieren, haben die Wissenschaftler in der "Naturstoff-abgeleiteten Synthese" zunächst zwei Naturstoff-Bibliotheken sowie 354 isolierte Naturstoffe der Firma AnalytiCon Discovery im biochemischen Screen auf folgende sieben Phosphatasen getestet – VE-PTP, Cdc25A, PTP1b, VHR, Shp-2, MptpA und MptpB:
- Die Inhibition von VE-PTP gilt als viel versprechender Ansatz für die Entwicklung von Antiangiogenese-Hemmern in der Krebstherapie.
- Cdc25A greift in die Regulation des Zellzyklus ein und gilt ebenfalls als interessantes Ziel in der Krebstherapie.
- Die Phosphatase MptpB aus Mycobacterium tuberculosis beeinflusst die Immunreaktion des Wirtes bei einer Tuberkuloseinfektion.
- VHR dephosphoryliert die MAP-Kinasen in der Aktivierungsschleife THX, die eine wichtige Rolle in Signaltransduktionsprozessen spielt.
- Die Hemmung von MptpB und Shp-2 erschließt neue Richtungen für die Suche nach Antiinfektiva.
- Das Enzym Ptp1B schließlich spielt eine wichtige Rolle bei der Entwicklung von Medikamenten gegen Diabetes Typ 2 und das metabolische Syndrom.
Die Auswahl der Naturstoffe und der Verbindungssammlungen beruhen auf dem Grundsatz, ein strukturell verschiedenes Screening-Set zu verwenden. Die Naturstoffbibliothek 1 (s. Abb. 1) besteht aus 1.271 Verbindungen auf Grundlage des Alkaloids Cytisin und lieferte Hemmstoffe für VE-PTP im niedrigen, mikromolaren Bereich. Für VE-PTP, das von der Arbeitsgruppe um Dietmar Vestweber am Max-Planck-Institut für molekulare Biomedizin stammt, waren es die ersten Inhibitoren überhaupt. Die Naturstoffbibliothek 2 (s. Abb. 1), die strukturell von den Furanodictinen abstammt, erwies sich als neue Inhibitor-Klasse für die Enzyme PTP1b und Shp-2. Die besten Inhibitoren lagen im niedrigen, mikromolaren Bereich und waren mindestens 20 Mal selektiver für Shp-2 als für die anderen, getesteten Phosphatasen.
Im Screening der 354 isolierten Naturstoffe erwiesen sich drei von sieben isolierten Yohimbin-Alkaloide (s. Abb. 1) als schwache Inhibitoren von Cdc25A. Legt man die Resultate der untersuchten ersten beiden Bibliotheken zugrunde, so könnte man auch hier durch entsprechende Strukturvariationen Verbindungen mit gesteigerter Aktivität erhalten. Aufgrund der strukturellen Komplexität dieser Alkaloide haben die Forscher das SCONP-Prinzip, welches die Naturstoffe in einer baumartigen Struktur anordnet und klassifiziert, als zweites Kriterium mit in ihre Untersuchung einbezogen und für die Strukturvereinfachung genutzt. Dazu ordneten sie die Grundstruktur der Yohimbin-Alkaloide 1 dem Indol-Zweig des SCONP-Baumes zu (s. Abb. 2).
Anschließend führte ein in der Baumstruktur wurzelwärts, also in Richtung einfacherer Grundgerüste gerichtetes "Schwingangeln" im SCONP-Baum zum tetracyclischen Indolochinolizidin-Grundgerüst 2 und über die tricyclischen tetrahydro-ß-carboline 3 zu den Indolen 4.
Nach dem Prinzip der "Naturstoff-inspirierten Synthese" wurden daraufhin 450 Indolochinolizidine auf polymerem Träger aufgebaut. Ein Screening dieser Verbindungen ergab zwei schwache Cdc25A-Inhibitoren, womit bewiesen ist, dass trotz struktureller Vereinfachungen von den pentacyclischen Alkaloiden zu den Indolochinolizidenen durch das SCONP-Prinzip die Aktivität für das gleiche Enzym erhalten bleibt.
Darüber hinaus zeigte sich aber, dass die Verbindungskollektion auch 11 Inhibitoren im niedrigen, mikromolaren Bereich für MptpB enthielt. Für MptpB, welches von der Arbeitsgruppe um Harald Schwalbe, Universität Frankfurt/Main, stammt, wurden ebenfalls zum ersten Mal Inhibitoren gefunden, die darüber hinaus noch außerordentlich selektiv waren. Von diesen 11 Verbindungen hemmten 9 ausschließlich MptpB. Auch die Bibliothek der 188 strukturell noch mehr vereinfachten Indole 4 zeigten diese Eigenschaften. Zwei der Verbindungen waren schwache Inhibitoren von Cdc25A – ähnlich wie der Naturstoff 1. Interessanterweise waren aber sieben der 188 Indole sogar nanomolare Inhibitoren von MptpB.
Diese Forschungsergebnisse zeigen eindrucksvoll, wie erfolgreich das Konzept der biologisch-orientierten Synthese für die gezielte Suche nach neuen Verbindungsklassen und für die Entwicklung neuartiger Therapeutika eingesetzt werden kann. [AN/AT]
Originalveröffentlichung:
Andrea Nören-Müller, Ivan Reis-Correa, Jr, Heino Prinz, Claudia Rosenbaum, Krishna Saxena, Harald J. Schwalbe, Dietmar Vestweber, Guiseppe Cagna, Stefan Schunk, Oliver Schwarz, Hajo Schiewe and Herbert Waldmann
Discovery of protein phosphatase inhibitor classes by biology-oriented synthesis
PNAS, Early Edition, 26 – 30 June 2006
Media Contact
Weitere Informationen:
http://www.mpg.de/Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Wasserabweisende Fasern ohne PFAS
Endlich umweltfreundlich… Regenjacken, Badehosen oder Polsterstoffe: Textilien mit wasserabweisenden Eigenschaften benötigen eine chemische Imprägnierung. Fluor-haltige PFAS-Chemikalien sind zwar wirkungsvoll, schaden aber der Gesundheit und reichern sich in der Umwelt an….

Das massereichste stellare schwarze Loch unserer Galaxie entdeckt
Astronominnen und Astronomen haben das massereichste stellare schwarze Loch identifiziert, das bisher in der Milchstraßengalaxie entdeckt wurde. Entdeckt wurde das schwarze Loch in den Daten der Gaia-Mission der Europäischen Weltraumorganisation,…

Neues Schweißverfahren für Windräder
… ermöglicht beschleunigte Produktion. Die Bundesanstalt für Materialforschung und -prüfung (BAM) stellt auf der diesjährigen Hannover Messe ein innovatives Schweißverfahren für Windräder vor, mit dem sich die Produktionsgeschwindigkeit von Windgiganten…