Einblicke in den dynamischen Aufbau der molekularen Spleißmaschine
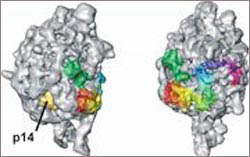
Zwei Ansichten der dreidimensionalen Struktur des U11/U12 di-snRNP, die mittels der dreidimensionalen Kryo-Elektronenmikroskopie bestimmt wurde. Einzelne Proteindomänen sind farblich hinterlegt. (Quelle: Stark/MPIbpc)
Wie aus der genetischen Information einer Zelle Proteine erzeugt werden, ist gegenwärtig ein zentrales Thema biochemischer Forschung. Eine besondere Rolle spielen dabei „Spleißosomen“, kleine molekulare Maschinen, die Stücke aus der RNA ausschneiden und neu aneinander heften. Wissenschaftlern am MPI für biophysikalische Chemie in Göttingen sind mit elektronenmikroskopischen Methoden jetzt erste Einblicke in den molekularen Aufbau eines Spleißosoms gelungen. (Molecular Cell, 18.3.2005)
Die genetische Information (DNA) in einer Zelle dient als Vorlage zur Synthese von Proteinen. Dabei wird zuerst die DNA in eine so genannte Boten-RNA (mRNA) übersetzt. Die Information der mRNA wird dann direkt für die Synthese von Proteinen verwendet. Ein wichtiger Schritt in dieser Kette vom Gen zum Protein ist die Prozessierung der mRNA in ein für die Synthese geeigneten, reifen Zustand. Dafür müssen Sequenzbereiche aus der so genannten prä-mRNA herausgeschnitten werden, die nicht für die Protein-Synthese vorgesehen sind. Dieses Herausschneiden wird beim Menschen von den so genannten Spleißosomen punktgenau durchgeführt. Diese Spleißosomen werden in einem hochdynamischen Assemblierungsweg aus kleineren Bausteinen zusammengesetzt, über den bisher auf dreidimensionaler Ebene wenig bekannt ist. Wissenschaftlern des Max-Planck-Instituts für biophysikalische Chemie ist es jetzt gelungen, die dreidimensionale Struktur eines der Hauptspieler des Spleißosoms zu bestimmen und so erste visuelle Einblicke in die frühen Assemblierungsschritte des Spleißosoms zu gewinnen.
Das Herausschneiden der für die Proteinsynthese nicht benötigten Sequenzen (Introns) und das Zusammenfügen der für die Proteinsynthese relevanten Sequenzen (Exons) wird in Analogie zum Verbinden von offenen Seilenden auch als „Spleißen“ bezeichnet. Das Spleißen stellt einen bedeutenden Prozess zur außerordentlichen Erhöhung der Proteinvielfalt dar, da durch unterschiedliche Verknüpfung und Überspringen von Exons verschiedene Proteine mit unterschiedlichen Eigenschaften aus einem einzelnen Gen erhalten werden können. Welche besondere Bedeutung das Spleißen für den Menschen hat, wird deutlich bei Betrachtung der Vielzahl von Krankheiten, die mit Fehlfunktionen des Spleißprozesses assoziiert sind. Hierzu zählen unter anderem bestimmte Formen der Retinitis pigmentosa, einer Krankheit, die zur Erblindung führen kann, die spinale Muskelatrophie Werdnig-Hoffmann, einer Erkrankung der Nervenzellen des Rückenmarks, die innerhalb der ersten Lebensjahre tödlich verlaufen kann, sowie bestimmte Formen von bösartigen Tumoren.
Für ein vertieftes Verständnis des Spleißvorganges und somit auch für die Möglichkeit, aus diesem Wissen neue therapeutische Ansätze zu entwickeln, ist es notwendig, die Funktion und Dynamik des zugrundeliegenden Prozesses zu kennen. Hierbei spielt die Bestimmung der dreidimensionalen Struktur eine wichtige Rolle. In einer früheren Studie (vgl. Pressemitteilung vom 26.05.2003) konnten Wissenschaftler des Max-Planck-Instituts bereits einen ersten Einblick in das Herz der molekularen Spleißmaschine gewinnen und einzelne Proteindichten zentralen Schlüsselproteinen zuordnen. Hierbei stellte sich heraus, dass eines der Proteine des so genannten Spleißfaktors 3b (SF3b), das sich direkt am katalytisch aktiven Zentrum des Spleißosoms befindet, im Inneren des Komplexes, vollständig umgeben von weiteren Proteindichten, lokalisiert ist. Diese bemerkenswerte Architektur des Komplexes warf die mechanistische Frage auf, wie die prä-mRNA in das Innere des Komplexes gelangen könnte. Wissenschaftler des Max-Planck-Institutes für biophysikalische Chemie in Göttingen konnten jetzt den Mechanismus auf der dreidimensionalen Ebene entschlüsseln.
In Zusammenarbeit mit Dr. Cindy Will aus der Abteilung von Prof. Reinhard Lührmann konnten Monika Golas und Björn Sander aus der Arbeitsgruppe von Dr. Holger Stark im Rahmen ihrer Doktorarbeiten die dreidimensionale Struktur des sogenannten U11/U12 di-snRNPs, eines der Hauptakeure des minoren Spleißosoms, mit einer Auflösung von etwa 1 Millionstel Millimeter mit Hilfe der Kryo-Elektronenmikroskopie bestimmen (Abbildung). Das Elektronenmikroskop wird hierbei, ähnlich wie bei der Computertomographie in der Medizin, zur Aufnahme von zweidimensionalen Projektionsbildern verwendet, die anschließend mittels in der Arbeitsgruppe neu entwickelter Computerprogramme in dreidimensionale Strukturen zurückgerechnet werden können. Aufgrund der hohen Auflösung konnten in dem nur maximal 26 Millionstel Millimeter großen Partikel direkt wichtige Proteine zugeordnet und ein Modell für den Aufbau der frühen Formen des Spleißosoms im Rahmen seiner Assemblierung entwickelt werden. Demnach liegt der Schlüssel zum Mechanismus der prä-mRNA-Bindung in einer Öffnung der Struktur des SF3bs. Hierdurch wird das zentrale Protein des SF3bs an die Oberfläche verlagert und kann so direkt mit der prä-mRNA interagieren. Zukünftige Studien sind zur Klärung geplant, wie und an welchen Schritten die struktuelle Änderung vorgenommen wird und welche Komponenten daran beteiligt sind.
Media Contact
Alle Nachrichten aus der Kategorie: Biowissenschaften Chemie
Der innovations-report bietet im Bereich der "Life Sciences" Berichte und Artikel über Anwendungen und wissenschaftliche Erkenntnisse der modernen Biologie, der Chemie und der Humanmedizin.
Unter anderem finden Sie Wissenswertes aus den Teilbereichen: Bakteriologie, Biochemie, Bionik, Bioinformatik, Biophysik, Biotechnologie, Genetik, Geobotanik, Humanbiologie, Meeresbiologie, Mikrobiologie, Molekularbiologie, Zellbiologie, Zoologie, Bioanorganische Chemie, Mikrochemie und Umweltchemie.
Neueste Beiträge

Nanofasern befreien Wasser von gefährlichen Farbstoffen
Farbstoffe, wie sie zum Beispiel in der Textilindustrie verwendet werden, sind ein großes Umweltproblem. An der TU Wien entwickelte man nun effiziente Filter dafür – mit Hilfe von Zellulose-Abfällen. Abfall…

Entscheidender Durchbruch für die Batterieproduktion
Energie speichern und nutzen mit innovativen Schwefelkathoden. HU-Forschungsteam entwickelt Grundlagen für nachhaltige Batterietechnologie. Elektromobilität und portable elektronische Geräte wie Laptop und Handy sind ohne die Verwendung von Lithium-Ionen-Batterien undenkbar. Das…

Wenn Immunzellen den Körper bewegungsunfähig machen
Weltweit erste Therapie der systemischen Sklerose mit einer onkologischen Immuntherapie am LMU Klinikum München. Es ist ein durchaus spektakulärer Fall: Nach einem mehrwöchigen Behandlungszyklus mit einem immuntherapeutischen Krebsmedikament hat ein…





















